Clinical Efficacy of Vinorelbine Combined with Xeloda for Patients with Anthracycline- and Taxane-refractory Metastatic Breast Cancer
-
摘要:目的 观察长春瑞滨(NVB)联合希罗达(XEL)21天方案([NX]方案), 治疗蒽环类和紫杉类药物耐药的转移性乳腺癌(anthracycline-and taxanerefractory metastatic breast cance, ATRMBC)患者的疗效和不良反应方法 NVB 25 mg/m 2d1, 8, 快速静滴; XEL2.0g/(m2·d), 早晚2次, 餐后30min口服, d1~14, 21天为1个疗程, 最多接受6个周期化疗或至疾病进展。结果 48例患者共完成172个周期化疗, 中位化疗周期4个周期均可评价疗效和不良反应其中完全缓解(CR)0例, 部分缓解(PR)11例, 稳定(SD)23例, 进展(PD)14例总有效率(CR+PR)22.92%, 疾病控制率(DCR)70.83%, 中位无进展生存期(TTP)6.7个月(1~22个月), 1年生存率.32/48(66.70%), 2年生存率21/48(43.75%)。治疗后主要不良反应为血液学毒性及手足综合征, 其次为胃肠道反应及脉管炎。结论 [NX]方案是治疗ATRMBC的有效方案, 不良反应可以耐受。Abstract:Objective This study aims to evaluate the clinical efficacy and tolerability of a three-week regimen of vinorelbine with xeloda for 48 patients with anthracycline- and taxane-refractory metastatic breast cancer(ATRMBC).Methods Forty-eight patients with anthracycline- and taxane-refractory metastatic breast cancer were enrolled in this study.All patients were given 25 mg/m 2 of vinorelbine on days one, and eight, combined with 2.0 g/m2 of xeloda daily from days 1 to 14.The combined chemotherapy was repeated every 21 days as one cycle.Patients received a maximum chemotherapy of six cycles or until disease progression.Results All 48 patients completed 172 chemotherapy cycles with a four-cycle median per patient.Adverse events and clinical efficacy were evaluated on all 48 patients.Complete remission(CR) was not observed in any patient, partial remission(PR) in 11 patients, stable disease(SD) in 23 patients, and progression of disease(PD) in 14 patients.The overall response rate(CR+PR) was 22.92%and the disease control rate (DCR) was 70.83%.The median time to progression(TTP) was 6.7 months(1 month to 22 months), 1-year survival rate was 66.70%, and two-year survival rate was 43.75%.The most commonly observed adverse events were hematologic toxicity and hand-foot syndrome, followed by gastrointestinal reaction and angeitis.No mortality occurred during the treatment.Conclusion Vinorelbine combined with xeloda is an effective and safe chemotherapeutic regimen for ATRMBC patients: the adverse reactions are well tolerated.
-
Keywords:
- Breast cancer /
- Vinorelbine /
- Xeloda /
- Drug tolerance
-
乳腺癌是世界范围内女性发病率最高的恶性肿瘤, 其发病率占全身各种肿瘤的7%~10%[1], 化疗迄今仍为乳腺癌的核心治疗方法, 而绝大数复发、进展的晚期乳腺癌不能被目前的治疗所治愈, 因此, 缓解病情、延长生存期及提高生存质量成为治疗的主要目的。近年大量研究报道长春瑞滨联合希罗达(NX)方案对于蒽环类、紫杉类治疗后复发转移乳腺癌有较高疗效[2], 本组资料回顾性分析本院与上海仁济医院2006年1月至2010年12月住院及门诊收治的48例晚期蒽环类和紫杉类耐药的乳腺癌患者应用[NX]方案治疗的疗效和不良反应, 以期为我国该类患者提供有益的治疗经验。
1. 材料与方法
1.1 一般资料
ATRMBC患者48例, 据病理证实浸润性导管癌43例, 浸润性小叶癌3例, 单纯癌1例, 炎性乳腺癌1例。其中骨转移29例, 肺转移25例, 肝转移23例, 脑转移9例(均合并脑外转移), 淋巴结转移19例, 软组织转移9例; 均有可测量病灶, 临床分期Ⅳ期复治患者。所有患者均为女性, 年龄31~80岁, 中位年龄53岁。病程11~192个月, 平均41个月。
1.2 入选标准
均经病理学细胞学证实的转移性乳腺癌患者; 对蒽环类和紫杉类药物耐药; 年龄≥18岁; 既往化疗未用XEL和NVB; 重要脏器功能基本正常; 预期生存期 > 3个月; KPS评分≥60分; 有客观评价病灶; 距末次化疗间隔≥4周; 所有患者结束蒽环类和紫杉类药物方案化疗至少2个周期, 停用化疗3个月内病情进展, 或在化疗过程中疾病进展。
1.3 治疗方法
NVB 25 mg/m2, d1, 8, 快速静滴; XEL 2.0 g/(m2·d), 早晚2次, 餐后30 min口服, dl~14, 21天为1个疗程, 最多接受6个周期化疗。连用2疗程后评价疗效。化疗前均有盐酸格拉司琼3 mg/d, 1~2次, 预防呕吐。
1.4 观察指标
化疗前每位患者进行体格检查, 必要的实验室检查(血、尿、粪常规, 肝、肾功能, 电解质等), 心电图, 影像学检查(B超、胸片、CT、骨扫描、MRI等)。化疗前详细记录病灶大小, 2个疗程化疗后重复以上检查。
1.5 疗效判定标准
疗效标准根据RECIST标准[3]评价疗效, 分为CR、PR、SD、PD, 有效率(RR)=CR+PR。疾病控制率(DCR)=CR+PR+SD。疼痛不适的改善作为治疗疗效的主要指标之一, 以止痛药物减少50%以上, 或主观评价法评定癌痛不适减轻为有效。肝、肾功能损伤作为治疗中对人体重要脏器的影响指标, 以生化检验结果为依据; 以统计学处理结论为准。生存质量评分, 治疗前后比较。治疗后较治疗前增加≥10分时为改善; 治疗后较治疗前减少≥10分为下降, 变化10分之内者为稳定。不良反应按WHO1981年统一标准评价。疾病进展时间(TTP)指化疗开始至疾病出现进展或死亡。
1.6 随访
随访时间为2006年1月至2011年6月。
1.7 统计学分析
采用SPSS 13.0统计软件包进行数据分析, TTP曲线采用Kaplan-Meier生存曲线分析获得, 用χ2检验比较组间差异, 以P < 0.05为差异有统计学意义。
2. 结果
2.1 近期疗效
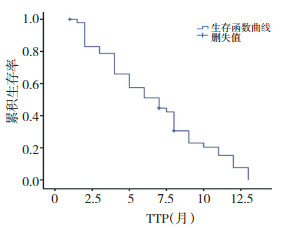
48例患者共完成172个周期化疗, 中位化疗周期4个周期。均可评价近期疗效和不良反应。CR0例, PR 1 1例, SD 23例, PD 14例。RR 22.92%, DCR70.83%, TTP 6.7个月(1~22个月)。至随访结束, 仍有7例患者生存。[NX]方案作为一、二线治疗, 其有效率分别为22.22%、23.23%, 差异无统计学意义。有效患者中, 有淋巴结及软组织转移者有效率最高(63.63%), 显著高于内脏转移者(P < 0.05), 肝、肺转移有效率无差异, 有脑转移者预后极差。各影响因素的亚组分析结果, TTP在年龄、ECOG评分、伴随转移灶数目及月经情况之间差异无统计学意义, 仅在转移部位之间差异有统计学意义(P < 0.05, 表 1)。TTP曲线(图 1)。
表 1 48例ATRMBC患者疗效及影响因素Table 1. Efficacy and influencing factors in this study
2.2 远期疗效
采用定期门诊、住院复查方式随访患者, 中断复查及失去联系者即视为死亡。48例患者1年总生存率为66.67%(28/48), 2年总生存率为38.89%(17/48)。截至2011年6月30日随访结束时, 死亡41例。
2.3 不良反应
该方案主要的不良反应为血液学毒性及手足综合征, Ⅰ~Ⅱ级血液学毒性发生率为62.50%, Ⅰ~Ⅱ级手足综合征发生率为60.42%。有4例因Ⅳ度血液学毒件化疗药物剂量减少25%, Ⅲ~Ⅳ级手足综合征为12.50%, 与Ciruelos等[4]报道相仿, 其中2例患者因1个周期治疗SD后因出现严重手足综合征要求更换方案(表 2)。
表 2 长春瑞滨联合希罗达化疗的不良反应 例(%)Table 2. Side-effects induced by the vinorelbine and xeloda regimen
2.4 疼痛不适及KPS改善情况
大部分患者疾病相关症状有不同程度的改善。KPS变化及疼痛不适改善均于治疗2个疗程结束后2周评价(表 3)。
表 3 生存质量及疼痛改善情况例 例Table 3. Quality of life and pain improvement
3. 讨论
目前, 蒽环类和紫杉类药物是目前治疗最有效方案之一[5], 已在全世界范围内得到广泛认同, 但药物在治疗中有20%~30%的患者会出现耐药性[6]。但是对于复发、进展及耐药性乳腺癌的治疗目前仍较棘手, 有研究表明, 蒽环类和紫杉类治疗后失败晚期乳腺癌患者再化疗有效率为33.0%~38.3%[7]。一般来说在姑息解救方案中应采用与蒽环类或紫杉类无交叉耐药且有效的方案。目前临床上推荐药物有吉西他滨、卡培他滨、长春瑞滨、顺铂等, 且联合治疗可能优于单药, 但无标准治疗方案。
希罗达也称为卡培他滨, 是经FDA批准的一类在肿瘤细胞内活化, 并可口服的氟化嘧啶类药物, 口服后可完整经胃肠道黏膜吸收, 后经3步独特的激活机制, 到达肿瘤组织后最终转化为5-Fu而发挥细胞毒作用[8]。目前研究表明, 单药希罗达口服疗效和任何5-FU静脉应用方法相媲美, 比静脉补液便捷, 并发症少。许多临床试验显示, 84%~89%的患者愿意选择口服化疗而非静脉化疗。
长春瑞滨是新型半合成的生物碱类药物, 通过阻滞微管蛋白的聚合, 使微管解聚而使细胞分裂停止于有丝分裂中期, 从而产生抗肿瘤作用且与蒽环类和紫杉类无交叉耐药[9]。长春瑞滨是单药治疗乳腺癌的有效药物, 据报道其一线治疗晚期乳腺癌有效率为36%, 二线为16%~45%。
临床资料显示, 希罗达和长春瑞滨联合应用有协同作用, 且无交叉耐药发生。大量国际Ⅰ、Ⅱ期临床试验显示希罗达联合长春瑞滨具有很高的疗效, 希罗达联合长春瑞滨治疗晚期乳腺癌的有效率为43%~67%。目前已经开始临床研究的希罗达联合方案包括多西紫杉醇、紫杉醇、长春瑞滨、赫塞汀等。本组48例患者RR 22.92%, DCR 70.83%, 疗效较好, 与文献报道相似[10], TTP 6.7个月, 1年生存率32/48 (66.70%), 2年生存率21/48 (43.75%)。[NX]方案作为一、二线治疗, 其有效率分别为22.22%、23.23%, 差异无统计学意义, 提示NX方案无论何时应用于乳腺癌, 均能显示较好的疗效。
-
表 1 48例ATRMBC患者疗效及影响因素
Table 1 Efficacy and influencing factors in this study

表 2 长春瑞滨联合希罗达化疗的不良反应 例(%)
Table 2 Side-effects induced by the vinorelbine and xeloda regimen

表 3 生存质量及疼痛改善情况例 例
Table 3 Quality of life and pain improvement

-
[1] 王天武. 多西他赛联合阿霉素治疗局部晚期乳腺癌疗效观察[J]. 实用肿瘤杂志, 2011, 26(3): 309-310. https://www.cnki.com.cn/Article/CJFDTOTAL-SYZZ201103037.htm [2] Nole F, Catanis C, Munzone E, et al. Catecitabine/vinorelbine: an effective and well-tolerated regimen for women with pretreated advanced-stage breast cancer[J]. Clin Breast Cancer, 2006, 6(6): 518-524. DOI: 10.3816/CBC.2006.n.005
[3] Jmeal A, Taylor T, Samuels A, et al. Cancer statistics, 2003[J]. CA Cancer J Clin, 2003, 53(1): 5-26. DOI: 10.3322/canjclin.53.1.5
[4] Ciruelos EM, Cortes J, Cortes-Funes H, et al. Gemcitabine and capecitabine in previously anthracycline-treated metastatic breast cancer: a multicenter phaseⅡstudy(SOLTI 0301 trial) [J]. Ann Oncol, 2010, 21(7): 1442-1447. DOI: 10.3322/canjclin.53.1.5
[5] Moulder S, Hortobaqyi GN. Advances in the treatment of breast cancer[J]. Clin Pharmacol Ther, 2008, 83(1): 26-36. DOI: 10.1038/sj.clpt.6100449
[6] 蔡晔芬, 伍俊妍. 盖诺联合卡培他滨治疗晚期乳癌临床观察[J]. 医学信息: 中旬刊, 2011, 24(7): 3094-3095. https://www.cnki.com.cn/Article/CJFDTOTAL-YXSS201107270.htm [7] Yardley DA. Activity of ixabepilone in patients with metastatic breast cancer with primary resistance to taxanes[J]. Clin Breast Cancer, 2008, 8(6): 487-492. DOI: 10.3816/CBC.2008.n.058
[8] 临床观察[J]. 中国医药导报, 2011, 8(15): 76-77. [9] 张军, 张西, 周从明, 等. 应用卡培他滨联合长春瑞滨治疗晚期乳腺癌的临床研究[J]. 中国伤残医学, 2011, 19(3): 35-36. https://www.cnki.com.cn/Article/CJFDTOTAL-XCYZ201103024.htm [10] 唐黎, 申剑, 武明花, 等. 卡培他滨联合长春瑞滨治疗复发转移性乳腺癌的临床观察[J]. 临床肿瘤学杂志, 2010, 15(1): 67-69. https://www.cnki.com.cn/Article/CJFDTOTAL-LCZL201001019.htm



 下载:
下载: