-
摘要: 腹膜种植转移是恶性肿瘤三大转移途径之一,也是临床肿瘤学长期认识不足、诊治技术水平落后的"老、大、难"问题。近30年,腹膜种植转移外科整合诊治技术体系的建立、完善和推广,引领了肿瘤腹膜转移基础、转化和临床研究热潮,推动形成了腹膜肿瘤学学科雏形,填补了临床肿瘤学的空白。基于对腹膜转移肿瘤生物学规律、特点和机制的深入认识,腹膜肿瘤临床诊断学、治疗学核心技术体系初步建成并逐渐完善,诞生了高级别循证医学证据导向的"十大里程碑"事件。2012年,《中国肿瘤临床》首推"腹膜转移癌专栏",引领国内肿瘤学界着力研究腹膜癌诊治策略。8年来,在中国抗癌协会的大力支持下,我国腹膜肿瘤学专家协同努力,逐步完善了中国特色的腹膜癌综合诊疗技术体系,出版了国内首部腹膜癌专著,制定2项腹膜癌诊治专家共识,在学科理论形成、研究平台建设、临床实践指南等方面,全面引领了国内腹膜肿瘤学学科发展。今年再度推出"腹膜转移癌研究"专栏,系统介绍我国腹膜癌领域的最新成果,促进临床肿瘤学的发展,推动腹膜肿瘤学学科建设。Abstract: Peritoneal seeding is one of the three primary forms of cancer metastasis. Significant adverse events are observed in such cases due to inadequate understanding and knowledge of peritoneal cancer. Over the past 30 years, the establishment, improvement, and promotion of surgery-based integrated diagnostic and treatment strategy for peritoneal metastasis have led to an increase in basic, translational, and clinical research. This has resulted in the formation of a new discipline, peritoneal surface oncology. Based on an in-depth understanding of the biological basis, characteristics, and mechanisms of peritoneal metastasis, core clinical diagnostic and therapeutic techniques have been established and improved. From this, the "Ten Milestones" of high-level evidence-based treatment progress has been established. In 2012, the Chinese Journal of Clinical Oncology first launched the "Special Column on Peritoneal Metastasis, " urging Chinese clinical oncologists to improve the diagnostic and therapeutic strategies for peritoneal carcinomatosis. Over the past 8 years, with full support from the China Anti-Cancer Association and from oncologists across the country, a comprehensive diagnostic and treatment system for peritoneal metastasis with Chinese characteristics has been established. The publication of the first monograph on this topic in Chinese and the formation of two expert consensuses have led to developments in discipline theory, research platform construction, clinical practice guidelines, and other aspects regarding peritoneal surface oncology in China. Once again, entrusted by the Chinese Journal of Clinical Oncology, we organized the special column "Highlights in Peritoneal Carcinomatosis" aiming to systematically summarize the latest achievements in the field of peritoneal cancer in China, promote the developments in clinical oncology, and provide an overview of the discipline of peritoneal surface oncology.
-
Keywords:
- peritoneal metastasis /
- clinical oncology /
- expert consensuses
-
众所周知,肿瘤学研究的两大主题是肿瘤如何发生、如何进展。基于对这两个问题深入研究所形成的认识,发展一系列防治技术体系,推动形成临床实践新范式,从而完成一次肿瘤学认识飞越和肿瘤诊治实践进步,是临床肿瘤学发展的必由之路。
肿瘤进展的表现形式就是侵袭和转移,而肿瘤转移则是恶性肿瘤的最本质特性。经典的肿瘤转移途径有三:淋巴道转移、血道转移、腹膜种植转移。梳理实体瘤现代临床治疗实践的发展历史脉络,可以清晰看到三个历史性飞越阶段。首先是针对淋巴道转移外科综合治疗技术体系的发展,其时代历程是1940年代到1980年,这个时期创建和发展了针对淋巴结转移的诊断分期和治疗技术,典型代表是大力提升了乳腺癌、胃癌和结直肠癌淋巴结转移的外科综合治疗能力。然后是针对血道转移外科综合治疗技术体系的发展,其时代历程是1960年到1990年,这个时期创建和发展了针对肿瘤肝转移、肺转移的诊断分期和外科综合治疗技术,经典代表是大力提升了肿瘤肝脏寡转移和肺脏寡转移的外科综合治疗能力。最后是针对腹膜种植转移外科综合治疗技术体系的发展,其时代历程是1980年到2010年,这个时期创建和发展了实体瘤腹膜转移的诊断分期和外科综合治疗技术,经典代表是大力提升了胃肠道肿瘤和妇科肿瘤腹膜转移外科综合治疗能力。因此,从历史和发展的角度来讲,临床肿瘤学的发展经历了从易到难、从常见到少见、从经验积累到学科发展的上升过程,直到近期,临床肿瘤学实践才形成完整学科框架,其发展之路仍然任重而道远。
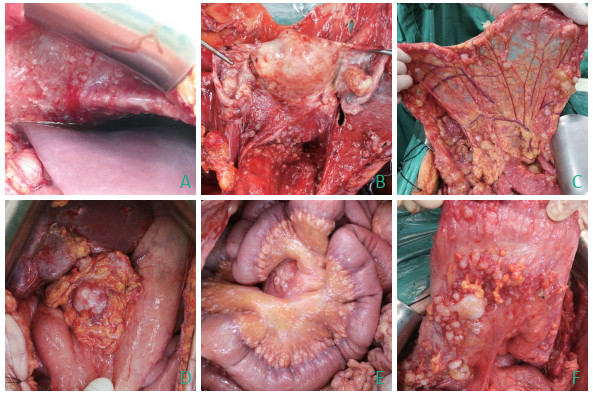
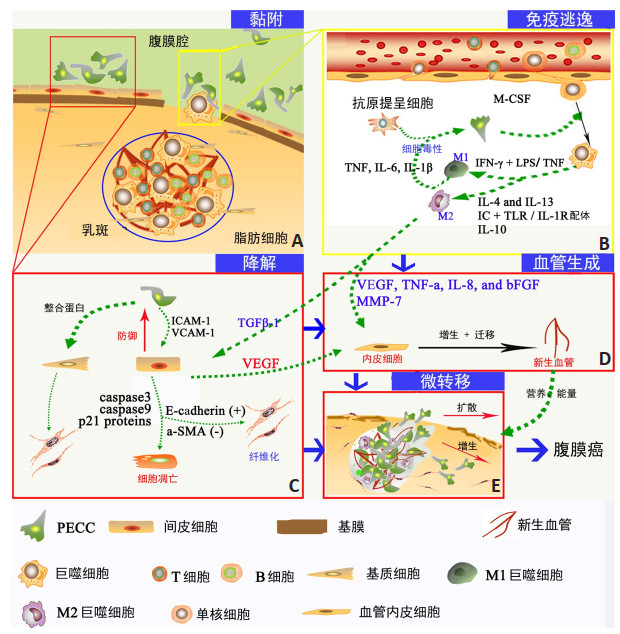
对肿瘤腹膜转移的深入研究,形成一系列全新认识,主要观点包括:1)腹膜转移有独特的肿瘤生物学规律和特点,其核心机制是癌细胞与腹膜表面特定结构乳斑的相互作用(图 1),形成有利于癌细胞在腹膜定植和增生的微环境[1];2)腹膜转移有特定的分布形式,集中分布于膈肌腹膜、盆腔腹膜、大小网膜、小肠系膜缘、大肠肠脂垂(图 2);3)腹膜转移有特殊的表现形式,三个经典表现是难治性腹水、顽固性腹痛、进展性肠梗阻[2];4)腹膜转移有准确的诊断学认识,这是一种区域性癌转移而非广泛的全身转移;5)腹膜转移有明确的治疗学技术策略,其核心是肿瘤细胞减灭术(cytoreductive surgery,CRS)加腹腔热灌注化疗(hyperthermic intraperitoneal chemotherapy,HIPEC)的外科整合治疗技术[3],腹腔化疗技术、分子靶向治疗技术,要点是强调区域控制、重视整体稳定。这些全新的临床肿瘤学认识深化和实践进步,构成了腹膜转移癌治疗的十大里程碑式进展[4-14](表 1),推动形成了腹膜肿瘤学学科(peritoneal surface oncology),其国际学术组织代表是腹膜表面肿瘤国际协作组联盟(Peritoneal Surface Oncology Group International,PSOGI),国内学术组织代表是中国抗癌协会腹膜肿瘤专业委员会(Peritoneal Surface Oncology Branch of China Anti-cancer Association)。
表 1 腹膜转移癌诊疗的十大里程碑事件
在中国抗癌协会的支持和领导下,我国的腹膜肿瘤学取得了长足发展,迅速缩短了与国际先进水平的差距,实现了从“跟跑到并跑到领跑”的历史性跨越,进入了中国腹膜肿瘤学发展的新时代。《中国肿瘤临床》是中国抗癌协会会刊,也是我国肿瘤学领域的旗舰杂志,始终敏锐把握我国肿瘤学最新进展,引领我国临床肿瘤学发展趋势。早在2012年就率先推出“腹膜转移癌治疗专栏”[2],全面介绍了国际的主要进展和国内研究现状,涵盖腹膜癌的分子机制、CRS+HIPEC临床前研究、诊断学研究、仪器设备开发以及临床研究等,不仅有助于提升我国腹膜癌综合防治的整体水平,还有力推动开展更高水平的循证医学研究。
时隔八年之后,《中国肿瘤临床》再次推出“腹膜转移癌研究专栏”,系统总结我国在腹膜肿瘤学领域的学科发展,并结合国际进展,提出未来的发展方向。
这八年中,我国腹膜癌诊治领域的突出进步就是形成了腹膜肿瘤学学科体系,涵盖了腹膜癌基础病理机制研究,新技术转化研究,临床应用研究,腹膜癌特效药物开发,适宜技术推广,人才培养和团队建设,学科理论发展等,取得了一系列可喜成果:1)在基础研究方面,建立了腹膜假黏液瘤[15]、腹膜恶性间皮瘤[16]、卵巢癌腹膜转移等体外研究平台和实验动物研究系统;2)在临床研究方面,开展围手术期安全性研究[17-18]、围手术期精细化管理研究[19],更加完善了腹膜癌综合诊疗技术体系;开展多中心、前瞻性临床研究,进一步明确腹膜癌综合诊疗技术临床疗效;3)在病理机制研究方面,开发腹膜癌量子点分子探针的可视化研究平台,人工智能的数字病理研究平台,基于全外显子测序和生物信息学分析技术的腹膜转移癌治疗新靶点检测和预后评估[20];4)在药物开发方面,开发并验证了阿霉素前体药、标准桃金娘油、阿帕替尼等腹膜癌特效药物;开展了全球首个针对腹膜癌的生物因子靶向药物(SCB-313)Ⅰ期临床试验项目,有望成为腹膜癌患者临床治疗的突破点;5)在技术推广方面,建设了北京市腹膜肿瘤学国际科技合作基地、“腹膜癌国际联盟•中国中心”和“欧洲腹膜癌学院·中国中心”、北京市肿瘤深部热疗与全身热疗技术培训基地,与挪威、日本、澳大利亚等国,以及国内主要腹膜癌诊治技术中心联合开展国际/国内多中心临床研究、青年医师培养、联合实验室建设、药物开发等;6)在人才培养方面,建设北京市腹膜肿瘤学优秀人才集体,获得北京市登峰人才培养计划支持,建立了人才培养定量评价系统[21],在全国范围内培养了大批临床、科研、教学、科普等全方位发展的腹膜肿瘤学专业化人才队伍;7)在学科理论建设方面,出版了《腹膜表面肿瘤细胞减灭术与围手术期化疗》专著[22],制订了《细胞减灭术加腹腔热灌注化疗治疗腹膜表面肿瘤的专家共识》[3],《肿瘤细胞减灭术加腹腔热灌注化疗治疗腹膜假黏液瘤专家共识》[23],《中国腹腔热灌注化疗技术临床应用专家共识(2019版)》[24],推动我国腹膜癌临床诊治和腹膜肿瘤学沿着严谨规范、科学实用的道路健康发展。
本期“腹膜转移癌研究专栏”收集了我国腹膜癌研究领域主要单位的最新成果,充分体现了我国腹膜肿瘤学专家始终走在临床肿瘤学实践前沿,创立和完善腹膜癌综合诊疗技术体系,从医、教、研全方位发展腹膜肿瘤学学科。在中国抗癌协会的支持和领导下,全国专家协同努力,我国的腹膜癌防治事业定会在新时代取得更大发展,为“健康中国”做出更大的贡献。
-
表 1 腹膜转移癌诊疗的十大里程碑事件

-
[1] Liu JY, Geng XF, Li Y. Milky spots:omental functional units and hotbeds for peritoneal cancer metastasis[J]. Tumour Biol, 2016, 37(5):5715-5726. DOI: 10.1007/s13277-016-4887-3
[2] 李雁.腹膜癌之我见[J].中国肿瘤临床, 2012, 39(22):1685-1686. DOI: 10.3969/j.issn.1000-8179.2012.22.001 [3] 李雁, 周云峰, 梁寒, 等.细胞减灭术加腹腔热灌注化疗治疗腹膜表面肿瘤的专家共识[J].中国肿瘤临床, 2015, 42(4):198-206. DOI: 10.3969/j.issn.1000-8179.20150013 [4] Spratt JS, Adcock RA, Muskovin M, et al. Clinical delivery system for intraperitoneal hyperthermic chemotherapy[J]. Cancer Res, 1980, 40:256-260. http://cn.bing.com/academic/profile?id=663330bc9eaba9d772fd329497cc0b7d&encoded=0&v=paper_preview&mkt=zh-cn
[5] Fujimoto S, Shrestha RD, Kokubun M, et al. Intraperitoneal hyperthermic perfusion combined with surgery effiective for gastric cancer patients with peritoneal seeding[J]. Ann Surg, 1988, 208(1):36-41. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1493580/
[6] Sugarbaker PH. Peritonectomy procedures[J]. Ann Surg, 1995, 221(1):29-42. DOI: 10.1097/00000658-199501000-00004
[7] Moran BJ, Cecil TD. The etiology, clinical presentation, and management of pseudomyxoma peritonei[J]. Surg Oncol Clin N Am, 2003, 12:585-603. DOI: 10.1016/S1055-3207(03)00026-7
[8] Verwaal VJ, van Ruth S, de Bree E, et al. Randomized trial of cytoreduction and hyperthermic intraperitoneal chemotherapy versus systemic chemotherapy and palliative surgery in patients with peritoneal carcinomatosis of colorectal cancer[J]. J Clin Oncol, 2003, 21(20):3737-3743. DOI: 10.1200/JCO.2003.04.187
[9] Baratti D, Kusamura S, Deraco M. The fifth international workshop on peritoneal surface malignancy (Milan, Italy, December 4-6, 2006):methodology of disease-specific consensus[J]. J Surg Oncol, 2008, 98(4):258-262. http://cn.bing.com/academic/profile?id=00653d07b8cfd6c0f44b060cc0ca914c&encoded=0&v=paper_preview&mkt=zh-cn
[10] Gomez PA, Kusamura S, Baratti D, et al. The intraoperative staging systems in the management of peritoneal surface malignancy[J]. J Surg Oncol, 2008, 98(4):228-231. http://cn.bing.com/academic/profile?id=205d2e934d803707ae9c95063b6b4d15&encoded=0&v=paper_preview&mkt=zh-cn
[11] Yang XJ, Huang CQ, Suo T, et al. Cytoreductive surgery and hyperthermic intraperitoneal chemotherapy improves survival of patients with peritoneal carcinomatosis from gastric cancer:final results of a phase III randomized clinical trial[J]. Ann Surg Oncol, 2011, 18(6):1575-1581. DOI: 10.1245/s10434-011-1631-5
[12] Li Y, Yu Y, Liu Y. Report on the 9th international congress on peritoneal surface malignancies[J]. Cancer Bio Med, 2014, 11(4):281-284. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgzllc-e201404008
[13] Lambert LA. Looking up:recent advances in understanding and treating peritoneal carcinomatosis[J]. CA Cancer J Clin, 2015, 65(4):283-298. DOI: 10.3322/caac.21277
[14] van Driel WJ, Koole SN, Sikorska K, et al. Hyperthermic intraperitoneal chemotherapy in ovarian cancer[J]. N Engl J Med, 2018, 378(3):230-240. DOI: 10.1056/NEJMoa1708618
[15] Lin YL, Zhang J, Yan FC, et al. Establishment of patient-derived xenograft model of peritoneal mucinous carcinomatosis with signet ring cells and in vivo study on the efficacy and toxicity of intraperitoneal injection of 5-fluorouracil[J]. Cancer Med, 2020, 9(3):1104-1114. http://cn.bing.com/academic/profile?id=fb0c2cc7dee0083578d7d054d000aab8&encoded=0&v=paper_preview&mkt=zh-cn
[16] 杨智冉, 林育林, 张珏, 等.恶性腹膜间皮瘤裸小鼠原位模型的建立及其生物学性状鉴定[J].中华病理学杂志, 2020, 49(2):162-167. DOI: 10.3760/cma.j.issn.0529-5807.2020.02.011 [17] Li XB, Ma R, Ji ZH, et al. Perioperative safety after cytoreductive surgery plus hyperthermic intraperitoneal chemotherapy for pseudomyxoma peritonei from appendiceal origin:experience on 254 patients from a single center[J]. Eur J Surg Oncol, 2020, 46(4 Pt A):600-606. http://cn.bing.com/academic/profile?id=8db0549d5163392148ba674b29116aa2&encoded=0&v=paper_preview&mkt=zh-cn
[18] Li XB, Peng KW, Ji ZH, et al. Prevention of venous thromboembolism after cytoreductive surgery and hyperthermic intraperitoneal chemotherapy:development of a physiotherapy program[J]. Clin Appl Thromb Hemost, 2019, 25:1076029619890415. http://cn.bing.com/academic/profile?id=037168fbb30c7d2ab33deed203e81073&encoded=0&v=paper_preview&mkt=zh-cn
[19] Liu G, Ji ZH, Yu Y, et al. Treatment of hypermyoglobinemia after CRS+HIPEC for patients with peritoneal carcinomatosis:a retrospective comparative study[J]. Medicine (Baltimore), 2017, 96(45):e8573. DOI: 10.1097/MD.0000000000008573
[20] Yan FC, Lin YL, Zhou Q, et al. Pathological prognostic factors of pseudomyxoma peritonei:comprehensive clinicopathological analysis of 155 cases[J]. Hum Pathol, 2020, 97:9-18. DOI: 10.1016/j.humpath.2019.12.008
[21] 林育林, 姬忠贺, 李鑫宝, 等.临床医师综合考评方法探析[J].中华医学教育杂志, 2018, 38(5):782-786. DOI: 10.3760/cma.j.issn.1673-677X.2018.05.033 [22] SugarbakerPH (主编), 李雁(主译).腹膜表面肿瘤细胞减灭术与围手术期化疗[M].第2版.北京: 科学出版社, 2018. [23] 李雁, 许洪斌, 彭正, 等.肿瘤细胞减灭术加腹腔热灌注化疗治疗腹膜假黏液瘤专家共识[J].中华医学杂志, 2019, 99(20):1527-1535. DOI: 10.3760/cma.j.issn.0376-2491.2019.20.003 [24] 中国抗癌协会腹膜肿瘤专业委员会, 广东省抗癌协会肿瘤热疗专业委员会.中国腹腔热灌注化疗技术临床应用专家共识(2019版)[J].中华医学杂志, 2020, 100(2):89-96. DOI: 10.3760/cma.j.issn.0376-2491.2020.02.003 -
期刊类型引用(4)
1. 李雁,姬忠贺. 论我国胃肠道癌腹膜转移诊治的难点和痛点. 中华胃肠外科杂志. 2023(05): 410-413 .  百度学术
百度学术
2. 姬忠贺,李雁. 肿瘤细胞减灭术加腹腔热灌注化疗治疗胃癌腹膜转移的现状与前景. 外科理论与实践. 2021(01): 11-16 .  百度学术
百度学术
3. 马茹,姬忠贺,张颖,李雁. 胃肠道癌腹膜转移的核心病理机制. 中华胃肠外科杂志. 2021(03): 198-203 .  百度学术
百度学术
4. 于洋,李鑫宝,林育林,马茹,姬忠贺,张彦斌,安松林,刘刚,杨肖军,李雁. 肿瘤细胞减灭术联合腹腔热灌注化疗治疗腹膜癌1 384例疗效分析. 中华胃肠外科杂志. 2021(03): 230-239 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载: