Treatment of advanced colorectal cancer with chemotherapy and recombinant human endostatin in the window period
-
摘要:目的 观察重组人血管内皮抑制素(恩度)窗口期联合化疗治疗晚期大肠癌的临床疗效。方法 选取2014年6月至2018年6月于贵州省肿瘤医院就诊的不可手术的晚期大肠癌患者120例,随机分为重组人血管内皮抑制素窗口期联合化疗组(试验组)及重组人血管内皮抑制素常规方案联合化疗组(对照组)各60例。试验组方案:重组人血管内皮抑制素15 mg/d,d1~d7,间歇7天重复,用药14天为1个周期,化疗于每周期使用重组人血管内皮抑制素第5天(窗口期)开始;对照组方案:重组人血管内皮抑制素15 mg/d,d1~d14,间歇7天重复,21天为1个周期,化疗于重组人血管内皮抑制素治疗第1天开始;两组均采用mFOLFOX6或FOLFIRI方案化疗。对比分析两组的临床疗效。结果 1)试验组与对照组客观有效率(objective response rate,ORR)分别为25.0%和18.3%,疾病控制率(disease control rate,DCR)分别为80.0%和73.3%,差异均无统计学意义(P=0.375,P=0.388);2)试验组与对照组1、2、3年生存率分别为(69.6% vs.62.5%)(39.7% vs.21.3%)(26.8% vs.13.3%),中位生存时间为22个月(95% CI:16.817~27.183)vs.16个月(95% CI:11.890~20.110),试验组较对照组生存率提高、生存时间延长,差异具有统计学意义(P=0.033)。3)试验组与对照组中位疾病进展时间(time to progression,TTP)分别为9、8个月,差异无统计学意义(P>0.05)。结论 重组人血管内皮抑制素窗口期联合化疗较常规应用方案联合化疗提高晚期大肠癌患者的1、2、3年生存率,延长中位生存时间。
-
关键词:
- 重组人血管内皮抑素/恩度 /
- 晚期大肠癌 /
- 重组人血管内皮抑素窗口期 /
- 化疗 /
- 疗效
Abstract:Objective To observe the effect of recombinant human endostatin (endostar) combined with chemotherapy on advanced colorectal cancer.Methods A total of 120 inoperable patients with advanced colorectal cancer who were admitted to the Guizhou Cancer Hospital from June 2014 to June 2018 were selected. The patients were divided into two groups. Sixty cases were allocated to the test group and received endostar of 15 mg/d, d1-d7, which was repeated after 7 and 14 days. Chemotherapy was initiated on the 5th day of endostar (endostar window period). Sixty patients were allocated to the control group and received endostar of 15 mg/d, d1-d14, which was repeated after 7 and 21 days. Chemotherapy was initiated on the 1st day of endostar. The chemotherapy regimen used was mFOLFOX6 or FOLFIRI.Results The objective response rate (ORR) of the test and control groups was 25.0%, and 18.3%, respectively, and the disease control rate (DCR) was 80.0% and 73.3%, respectively. The difference was not significant (P=0.375, P=0.388). The 1-year survival rate of the test group and the control group was 69.6% and 62.5%, respectively, while the 2-year survival rate was 39.7% and 21.3%, respectively. Moreover, the 3-year survival rate was 26.8% and 13.3%, respectively, and the median survival time was 22 months (95% CI 16.817-27.183) and 16 months (95% CI 11.890-20.110), respectively. In contrast to the control group, the survival rate increased and the survival time was prolonged in the test group (P=0.033). The progression time (TTP) of median disease in the test and control groups was 9 months and 8 months, respectively. This was not statistically significant (P>0.05).Conclusion This study found that chemotherapy with recombinant human endostatin in the window stage can enhance the 1, 2, and 3-year survival rate of patients with advanced colorectal cancer, as well as prolong the median survival time. -
化疗是晚期结直肠癌的主要治疗手段,联合分子靶向药物治疗可进一步提高晚期结直肠癌的疗效。NCCN(2007年)结直肠癌临床指南中推荐,抗血管生成药物贝伐单抗为晚期结直肠癌的一线治疗。贝伐单抗价格昂贵,多数晚期大肠癌患者难以自费使用。重组人血管内皮抑制素(恩度)是中国自主研发抗血管生成药物,推荐用于晚期非小细胞肺癌[1]。赖军明等[2]Meta分析结果显示,重组人血管内皮抑制素联合化疗治疗晚期大肠癌的近期疗效优于单纯化疗。重组人血管内皮抑制素于2010年进入贵州省晚期大肠癌乙类医疗保险(医保编号:810851054801),通过贵州省肿瘤医院伦理委员会审查后进入临床研究。闻杨等[3]研究结果显示,重组人血管内皮抑制素联合化疗治疗晚期大肠癌较单纯化疗具有较高的疾病控制率,并提高了生存率。重组人血管内皮抑制素常规使用方案(说明书推荐方案)为7.5 mg/m2/d,连用14天,休息7天重复。目前优化抗血管生成药物联合化疗的治疗方案是否可以增加晚期大肠癌疗效的研究报道较少。本研究旨在观察重组人血管内皮抑制素窗口期联合化疗治疗晚期大肠癌的临床疗效。
1. 材料与方法
1.1 病例资料
2014年6月至2018年6月贵州省肿瘤医院共收治的晚期大肠癌患者520例。纳入标准:1)年龄≥18岁,性别不限;2)组织学或/和细胞学证实为直肠癌或结肠癌;3)晚期不可手术结直肠癌,包括不能根治手术的初治转移性结直肠癌,根治术后转移性结直肠癌及根治术后辅助化疗或/和放疗后转移性结直肠癌不能再手术者;4)至少有一个双径可测量病灶;5)体力状况尚好,卡氏评分(KPS)为60~100分;6)预计生存期≥3个月;7)器官功能良好;8)自愿入组,依从性好,不采用贝伐单抗、西妥昔单抗治疗。均签署知情同意书。排除标准:1)妊娠,哺乳期妇女;2)伴严重心脏疾病及顽固性高血压;3)伴恶性浆膜腔积液;4)中枢神经转移瘤;5)机体上有未愈合的创伤;6)机体上有活动性出血;7)同时参加其他临床实验。根据上述标准,共纳入120例患者,随机分为重组人血管内皮抑制素窗口期联合化疗(试验组)60例与重组人血管内皮抑制素常规应用方案联合化疗(对照组)60例。本研究通过医院伦理委员会批准。
1.2 方法
1.2.1 重组人血管内皮抑制素治疗方案
对照组:重组人血管内皮抑制素15 mg/d,d1~d14,间歇7天重复,21天为1个周期,使用3~4个周期,化疗于重组人血管内皮抑制素治疗第1天开始。试验组:重组人血管内皮抑制素15 mg/d,d1~d7,间歇7天重复,用药14天为1个周期,使用3~4个周期。化疗于每周期使用重组人血管内皮抑制素第5天(窗口期)开始,因化疗不良反应需延迟下一周期化疗,重组人血管内皮抑制素顺延治疗。
1.2.2 化疗
两组患者均采用mFOLFOX6或FOLFIRI方案化疗,每14天重复,2次化疗为1个周期。mFOLFOX6方案:奥沙利铂为85 mg/m2,静脉滴注2~6 h,d1;亚叶酸钙为400 mg/m2静脉滴注2 h,d1;5-Fu为400 mg/m2静脉推注于亚叶酸钙后,2 400 mg/m2持续静脉泵入46 h。FOLFIRI方案:伊立替康:UGT1A1为6/6、6/7型的患者的剂量选用180 mg/m2,UGT1A1为7/7型的患者选用150 mg/m2,静脉滴注30~90 min,d1;5-Fu用法同mFOLFOX6方案。化疗方案选择原则:首次就诊时为Ⅳ期、未行任何抗肿瘤相关治疗患者选用mFOLFOX6方案,既往根治术后接受奥沙利铂方案辅助化疗的患者选用FOLFIRI方案。
1.2.3 放疗
针对结直肠原发病灶及骨转移非靶病灶予以姑息减症放疗。直肠病灶放疗剂量为61.2 Gy/34次;结肠病灶放疗剂量50.4 Gy/28次;骨转移病灶放疗剂量30 Gy/10次。
1.2.4 疗效及不良反应评价
采用实体瘤RECIST 1.0标准评价即刻疗效。每4~6次化疗结束评价疗效1次,以完全缓解(complete response,CR)+部分缓解(partial response,PR)计算客观有效率(objective response rate,ORR),以CR+PR+稳定(stable disease,SD)计算疾病控制率(disease control rate,DCR)。总生存期(overall survival,OS)为从随机分组开始直至死亡或末次随访时间。疾病进展时间(time to progression,TTP)指从随机分组开始至肿瘤客观进展的时间。不良反应评估:按照NCI-CTC 3.0标准分为Ⅰ~Ⅴ级。第1周期使用重组人血管内皮抑制素前及末次使用后进行心电图、心脏B超及心功能、心肌酶学检查,余每周期使用前后只复查心电图。
1.2.5 随访
自治疗结束开始,每3个月随访1次,采用门诊复查及电话随访。内容包括病史询问、体格检查、癌胚抗原、糖类抗原、影像学复查(胸、腹、盆腔CT或MRI)。随访截止至2018年12月,失访4例,中位随访时间16.0个月,随访率96.7%。随访中发现试验组及对照组各1例出现肠梗阻并进行手术。
1.3 统计学分析
采用SPSS 17.0软件进行统计学分析。采用χ2检验比较ORR、DCR,采用Kaplan-Meier法绘制生存曲线,组间的生存比较采用Log-rank检验。计数资料采用率(%)表示。以P < 0.05为差异具有统计学意义。
2. 结果
2.1 一般资料
120例患者中,中位年龄为58岁。试验组男性44例、女性16例;对照组男性40例、女性20例。两组均以晚期直肠癌病例为主,以肝转移多见,转移病灶数目以多个为主。两组患者性别、年龄、原发肿瘤部位、病理类型、转移部位、转移器官数量、化疗方案等基线资料比较差异无统计学意义(P>0.05,表 1)。
表 1 患者一般资料
2.2 治疗完成情况
两组患者均完成2个周期以上重组人血管内皮抑制素治疗及化疗,试验组25例患者完成2~3个周期化疗,35例患者完成4~6个周期化疗;对照组23例患者完成2~3个周期化疗,37例完成4~6个周期化疗(表 2)。试验组行直肠原发病灶放疗9例,结肠原发病灶放疗2例,骨转移灶放疗2例;对照组行直肠原发病灶放疗6例,结肠原发病灶放疗2例,骨转移灶放疗3例。治疗中试验组1例乙状结肠癌肝转移经治疗后转化为可切除病灶,接受原发病灶及肝转移灶手术治疗,术后完成辅助化疗。
表 2 试验组及对照组治疗完成情况例 
2.4 近期疗效
两组患者均进行系统疗效评价,其中试验组CR、PR、SD、疾病进展(progressive disease,PD)分别为1、14、33、12例,对照组CR、PR、SD、PD分别为0、11、33、16例;试验组及对照组ORR分别为25.0%、18.3%,DCR分别为80.0%、73.3%(均P>0.05,表 3)。
表 3 试验组及对照组疗效对比
2.5 远期疗效
120例患者的1、2、3年生存率分别为66.0%、30.5%、20.6%;中位生存时间为19个月。
2.5.1 试验组与对照组生存比较
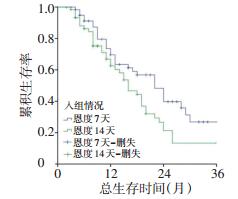
试验组与对照组的1年生存率分别为69.6%、62.5%,2年生存率分别为39.7%、21.3%,3年生存率分别为26.8%、13.3%,中位生存时间分别为22个月(95%CI:16.817~27.183)与16个月(95%CI:11.890~20.110),差异具有统计学意义(χ2= 4.551,P=0.033,图 1)。
2.5.2 试验组与对照组中重组人血管内皮抑制素联合FOLFOX方案化疗生存比较
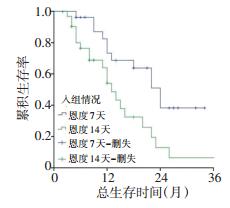
重组人血管内皮抑制素联合FOLFOX方案治疗共49例,1、2、3年生存率分别为63.0%、25.8%、22.6%,中位生存时间为18个月。其中,试验组27例、对照组22例,1年生存率分别为73.3%、50.4%,2年生存率分别为38.3%、13.0%,3年生存率分别为38.3%、6.5%,中位生存时间分别为24个月(95%CI:18.628~29.372)、13个月(95%CI:10.008~15.992),差异具有统计学意义(χ2=7.584,P=0.006,图 2)。
2.5.3 试验组与对照组中重组人血管内皮抑制素联合FOLFIRI方案化疗生存比较
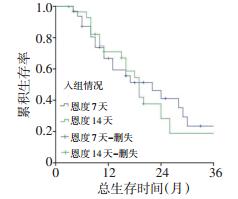
重组人血管内皮抑制素联合FOLFIRI方案化疗共71例,1、2、3年生存率分别为68.8%、34.3%、21.1%,中位生存时间为19个月。其中,试验组33例,对照组38例,1年生存率分别为66.7%、70.9%,2年生存率分别为41.1%、28.3%,3年生存率分别为23.5%、18.8%,中位生存时间分别为22个月(95% CI:11.393~32.607)、19个月(95%CI:15.530~22.470),差异无统计学意义(χ2=0.108,P=0.742,图 3)。
2.5.4 试验组与对照组TTP比较
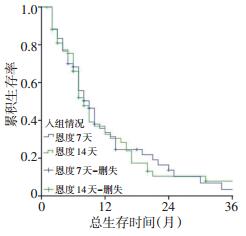
全组120例患者TTP为8个月。试验组与对照组的TTP分别为9、8个月,差异无统计学意义(χ2=0.052,P=0.819,图 4)。
2.6 不良反应
两组患者主要不良反应均表现为血液学毒性、胃肠道反应、肝功能异常及心脏毒性,多为Ⅰ~Ⅱ级,Ⅲ~Ⅳ级反应发生率低,一般经对症治疗可恢复正常,未发生较重的心血管系统等不良反应,未发生治疗相关性临床死亡事件。两组不良反应比较差异无统计学意义(P>0.05,表 4)
表 4 试验组与对照组不良反应比较
3. 讨论
1971年Folkmam[4]提出肿瘤血管生成是肿瘤生长、浸润和转移的必备条件。阻断肿瘤新生血管生成即可阻断肿瘤的发生发展。抗肿瘤血管生成药物贝伐单抗联合化疗治疗晚期大肠癌较单纯化疗明显延长患者生存时间[5]。有研究表明[6]重组人血管内皮抑制素联合氟尿嘧啶具有协同作用,并可以抑制大肠癌的肝转移。另有研究报道[7-9],重组人血管内皮抑制素联合化疗治疗晚期大肠癌,无论是与FOLFOX/XELOX,还是FOLFIRI方案联合,较单纯化疗均具有较好的临床疗效。
有研究提出肿瘤血管正常化理论,肿瘤血管的正常化期为“窗口期”,在此时间内肿瘤细胞对化疗药物更加敏感[10-11]。有研究证明,重组人血管内皮抑制素能够使肺癌血管正常化,血管正常化的“时间窗”为用药开始的第5天左右,联合使用放疗或化疗可发挥最大抗肿瘤作用[12]。另有研究显示,重组人血管内皮抑素对小鼠胃癌移植瘤的血管正常化“时间窗”为用药后5~ 9天[13]。重组人血管内皮抑制素联合窗口期化疗明显提高治疗肺鳞癌ORR及DCR[14]。目前尚未见大肠癌中血管正常化“窗口期”联合化疗的相关基础研究报道,临床研究报道亦较少。本研究根据肿瘤血管正常化理论及晚期结直肠癌mFOLFOX6或FOLFIRI化疗方案14天重复的周期性特点,设计于每个周期重组人血管内皮抑制素窗口期联合化疗,结果显示ORR、DCR较对照组提高,差异无统计学意义(P>0.05);远期疗效方面,试验组较对照组具有更好的1、2、3年OS及中位生存时间(P < 0.05),考虑可能与重组人血管内皮抑制素窗口期内肿瘤血管趋于正常化,可更加有效地运输药物和氧到肿瘤细胞,进一步提高化疗的敏感性有关。本研究全组TTP为8个月,试验组较对照组延长,但差异无统计学意义,与既往报道[15]相近。本研究中重组人血管内皮抑制素联合mFOLFOX6方案的1、2、3年生存率分别为63.0%、25.8%、22.6%,中位生存时间为18个月,高于既往报道[7, 16],且试验组疗效明显高于对照组,提示该方案可能具有更好的生存获益。本研究两组患者共71例使用重组人血管内皮抑制素联合FOLFIRI方案治疗,1、2、3年生存率分别为68.8%、34.3%、21.1%,中位生存时间达19个月,高于既往报道[9],且试验组疗效高于对照组,考虑可能与本研究中重组人血管内皮抑制素窗口期联合化疗有关,两组差异无统计学意义,尚需进一步临床研究证实该方案是否更具生存优势。
重组人血管内皮抑制素Ⅲ期临床试验中显示的不良反应主要表现为心脏毒性,包括窦性心动过速、STT改变、房室传导阻滞、房性早搏和偶发室性早搏等,多见于有冠心病和高血压史的患者,程度均较轻,未发生Ⅳ级不良反应[2]。本研究中主要不良反应为骨髓抑制、胃肠道反应、肝肾功能异常及心脏毒性,多为Ⅰ~Ⅱ级,两组Ⅲ~Ⅳ级反应发生率均较低,无治疗相关性临床死亡事件发生,与重组人血管内皮抑制素联合化疗治疗转移性结直肠癌的既往报道相似[3, 7-9]。
综上所述,本研究结果表明,重组人血管内皮抑制素窗口期联合化疗较常规使用方案联合化疗提高晚期大肠癌的1、2、3年生存率,延长中位生存时间,值得临床进一步研究及推广应用。
-
表 1 患者一般资料

表 2 试验组及对照组治疗完成情况
例 
表 3 试验组及对照组疗效对比

表 4 试验组与对照组不良反应比较

-
[1] 王金万, 孙燕, 刘永煜, 等.重组人血管内皮抑素联合NP方案治疗晚期NSCLC随机、双盲、对照、多中心Ⅲ期临床研究[J].中国肺癌杂志, 2005, 8(4):283-290. http://d.old.wanfangdata.com.cn/Periodical/zgfazz200504007 [2] 赖军明, 罗辉, 林红, 等.晚期大肠癌重组人血管内皮抑制素联合化疗近期疗效和安全性Meta分析[J].中华肿瘤防治杂志, 2017, 24(22):1604-1610. http://d.old.wanfangdata.com.cn/Periodical/qlzlzz201722012 [3] 闻杨, 董洪敏, 王文玲, 等.重组人血管内皮抑制素联合化疗对晚期结直肠癌的疗效[J].中国现代医学杂志, 2018, 28(30):109-114. http://d.old.wanfangdata.com.cn/Periodical/zgxdyxzz201830022 [4] Folkmam J. Tumor angiogenesis:therapeutic implication[J]. N Engl J Med, 1971, 285(21):1182-1186. http://d.old.wanfangdata.com.cn/NSTLQK/NSTL_QKJJ0228010074/
[5] Hurwitz H, Fehrenbacher L, Novotny W, et al. Bevacizumab plus irinotecan, fluorouracil, and leucovorin for metastatic colorectal cancer[J]. N Engl J Med, 2004, 350(23):2335-2342. http://cn.bing.com/academic/profile?id=d620483f5e48b0ed9c9bef214ec1ecac&encoded=0&v=paper_preview&mkt=zh-cn
[6] 周志伟, 万德森, 王国强, 等.血管生成抑制剂YH-16抑制结肠癌肝转移的研究[J].癌症, 2006, 25(7):818-822. http://d.old.wanfangdata.com.cn/Periodical/ez200607006 [7] 綦晓艳, 余宗阳, 欧阳学农, 等.重组人血管内皮抑制素联合化疗一线治疗晚期转移性结直肠癌的疗效观察[J].现代肿瘤医学, 2015, 23(17):2459-2463. http://d.old.wanfangdata.com.cn/Periodical/sxzlyx201517021 [8] 和光宇.恩度联合化疗治疗晚期结肠癌临床分析[J].临床医学研究与实践, 2016, 1(2):41-41. http://d.old.wanfangdata.com.cn/Periodical/lcyxyjysj201602027 [9] Li BL, Hu XL, Zhao XH, et al. Endostar combined with irinotecan/calcium folinate/5-fluorouracil (FOLFIRI) for treating advanced colorectal cancer:A clinical study[J]. J Chemother, 2015, 27(5):301-306. http://cn.bing.com/academic/profile?id=de5f32440ee661ac46b3dc396b885827&encoded=0&v=paper_preview&mkt=zh-cn
[10] Jain RK. Normalizing tumor vasculature with anti-angiogenic therapy:a new paradigm for combination therapy[J]. Nat Med, 2001, 7(9):987-989. DOI: 10.1038-nm0901-987/
[11] Jain RK. Normalization of tumor vasculature:An emerging concept in antiangiogenic therapy[J]. Science, 2005, 307(5706):58-62. DOI: 10.1126-science.1104819/
[12] Ning T, Jiang M, Peng Q, et al. Low-dose endostatin normalizes the structure and function of tumor vasculature and improves the delivery and anti-tumor efficacy of cytotoxic drugs in a lung cancer xenograft murine model[J]. Thoracic Cancer, 2012, 3(3):229-238. http://cn.bing.com/academic/profile?id=2c175ea0bdb73b61b1b9ab827da37c33&encoded=0&v=paper_preview&mkt=zh-cn
[13] 郝美丽, 陈士花, 谭叶, 等.重组人血管内皮抑素对肿瘤血管正常化时间窗的研究[J].肿瘤学杂志, 2019, 25(11):962-965. http://d.old.wanfangdata.com.cn/Periodical/zlxzz201911008 [14] 胡代菊, 胡晓文, 汪萤.重组人血管内皮抑素静脉泵入联合窗口期化疗治疗晚期肺鳞癌的临床观察[J].临床肺科杂志, 2018, 23(6):1030-1034. http://d.old.wanfangdata.com.cn/Periodical/lcfkzz201806017 [15] 周彤, 徐建忠, 李苏宜, 等.恩度联合FOLFOX4方案治疗晚期结肠癌、直肠癌的多中心临床研究[J].实用临床医药杂志, 2012, 16(5):26-28. http://d.old.wanfangdata.com.cn/Periodical/jslcyxzz201205009 [16] 杜春霞, 杨林, 周爱萍, 等.重组人血管内皮抑素联合一线化疗治疗晚期结直肠癌的临床观察[J].中国肿瘤临床与康复, 2015, 22(9):1029-1033. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgzllcykf201509002



 下载:
下载: